Перейти к:
Определение индикативных показателей для организации мониторинга источников питьевого водоснабжения при изменении климатических условий
https://doi.org/10.35627/2219-5238/2022-30-9-84-90
Аннотация
Введение. В условиях ухудшения экологической обстановки водоемов необходимо создание системы мониторинга за изменяющимися показателями, которые могут повлиять на качество природной и подаваемой населению питьевой воды. Органический углерод выступает одним из индикативных показателей, отражающих скорость продукции и деструкции, климатические и техногенные воздействия, безопасность и эффективность очистки питьевой воды.
Цель исследования: изучение индикативных показателей при организации мониторинга источников питьевого водоснабжения.
Материалы и методы. В 2020–2021 гг. проводился ежемесячный отбор воды в источнике хозяйственно-питьевого водоснабжения крупного промышленного города Свердловской области и после водоочистки. Выполнялись измерения температуры воды, лабораторные исследования показателей: растворенный углерод (Cобщ, Cорг, Cнеорг), pH, перманганатная окисляемость (ПО), жесткость, сухой остаток. Проведен корреляционный анализ между показателями, оценена эффективность водоочистки.
Результаты. Максимальные концентрации Cобщ (54,3 мг/дм3) и Cорг (36,0 мг/дм3) в воде из водохранилища обнаружены в январе 2021 г. Преобладание концентраций Cнеорг по сравнению с Cорг установлено преимущественно в теплые месяцы. Водоподготовка обеспечивала снижение содержания Cобщ в питьевой воде на 12–32 %, Cорг – на 12–47 %, Cнеорг – на 6–32 %, ПО – на 28–68 % за исключением нескольких месяцев. В весенне-летний период 2021 г. обнаружено снижение ПО в водохранилище; повышение pH воды по сравнению с другими сезонами выявлено в летний период. Выявлена отрицательная корреляция между концентрациями Сорг и температурой воды.
Выводы. Организованы мониторинговые исследования поверхностного источника питьевого водоснабжения. Установлены сезонные закономерности изменения углерода и показателей минерального состава воды, показана эффективность водоподготовки.
Для цитирования:
Хлыстов И.А., Харькова П.К., Бугаева А.В., Замолоцких Т.В., Штин Т.Н., Гурвич В.Б. Определение индикативных показателей для организации мониторинга источников питьевого водоснабжения при изменении климатических условий. Здоровье населения и среда обитания – ЗНиСО. 2022;(9):84-90. https://doi.org/10.35627/2219-5238/2022-30-9-84-90
For citation:
Khlystov I.A., Kharkova P.K., Bugaeva A.V., Zamolotskikh T.V., Shtin T.N., Gurvich V.B. Determination of Key Quality Indicators for Organization of Potable Water Source Monitoring under Changing Climatic Conditions. Public Health and Life Environment – PH&LE. 2022;(9):84-90. (In Russ.) https://doi.org/10.35627/2219-5238/2022-30-9-84-90
Введение. Возрастающие антропогенные климатические изменения в будущем могут привести к появлению веществ с неизученными свойствами, ухудшению качества и дефициту питьевой воды, что неминуемо отразится на здоровье человека. Происходящие глобальные процессы выражаются в изменении количества осадков [1], увеличении подвижности загрязняющих веществ в пресноводных системах [2], трансформации биогеохимических циклов и, в частности, изменении активности микроорганизмов [3]. Увеличивающаяся водная и ветровая эрозия приведет к потерям почвенного углерода, вымыванию его в водоемы [4]. На территории Урала за последние 50 лет зафиксирован положительный тренд средней годовой температуры [5]. В водоемах часто обнаруживаются различные не характерные для естественной среды соединения, такие как пестициды, фунгициды, нефтепродукты, фенолы, полиароматические углеводороды [6[[7].
Одним из ключевых показателей, характеризующих равновесие скоростей продукции и деструкции [8], состояние источников водоснабжения, безопасность питьевой воды и эффективность ее очистки [9], выступает органический углерод. Основная опасность от присутствия в поступающей на хлорирование воде органического углерода связана с образованием токсичных побочных галогенированных продуктов [10]. При изучении органической составляющей водоемов нами была установлена связь между побочными образующимися галогенорганическими соединениями и влияющими на их образование предикторами: температура воды, pH, ионы аммония, общий органический углерод, общая щелочность, хлор остаточный суммарный, доза хлора на первичное и окончательное хлорирование, время хлорирования [9]. Для дальнейших исследований происходящих в водоемах процессов из данного перечня предикторов было выбрано три параметра: температура воды, pH, органический углерод. В условиях существующей опасности изменения физико-химического и биологического состава воды питьевых водоисточников и, как следствие, возникновения угрозы здоровью появляется необходимость организации мониторинговых исследований.
Цель исследования: изучение индикативных показателей при организации мониторинга источников питьевого водоснабжения.
Материалы и методы. В период с августа 2020 по август 2021 г. проводился ежемесячный отбор проб воды с двух точек: поступающая с поверхностного хозяйственно-питьевого источника (водохранилище) на станцию водоподготовки, вода после водоочистки (питьевая вода) крупного промышленного города Свердловской области. Температура воды измерялась в момент отбора. В обоих видах вод были исследованы показатели: массовые концентрации общего растворенного углерода (Cобщ), растворенного органического углерода (Cорг) и растворенного неорганического углерода (Cнеорг) на анализаторе общего углерода TOC-L Shimadzu; водородный показатель pH; перманганатная окисляемость (ПО); жесткость (титриметрически; по кальцию и магнию); сухой остаток (общая минерализация). Оценена эффективность водоподготовки. Все исследования выполнены на базе ОФХМИ ФБУН ЕМНЦ ПОЗРПП Роспотребнадзора. Отбор образцов и выполнение лабораторных исследований осуществлялись аттестованными методами, внесенными в реестр Росаккредитации. Расчет корреляций (критерий Спирмена) выполнен в Statistica 6. Результаты за весь период исследований рассчитаны в виде минимальных, максимальных и средних значений показателей; количество ежесезонных измерений показателей (осень 2021 – лето 2021 гг.) трехкратное.
Результаты. Температура воды в водохранилище соответствуют сезонным изменениям: максимальные значения выявлены в августе 2021 г., минимальные – в декабре 2020 г. Значения физико-химических показателей за период исследований представлены в табл. 1 и на рисунке, их среднесезонные значения – в табл. 2. Максимальные концентрации Cобщ и Cорг в водохранилище и питьевой воде выявлены в январе 2021 г., минимальные значения этих показателей приходятся на осень 2020 и весну 2021 г. Максимальная концентрация Cнеорг в воде водохранилища и питьевой воде выявлена в январе 2021 г. Наибольшее отношение концентраций Cорг/Cнеорг установлено в период с декабря по апрель: для природной воды оно находилось в пределах 1,3–3,3, для питьевой воды – 1,0–4,3. Преобладание концентрации Cнеорг над Cорг выявлено с сентября по ноябрь 2020 г. и с мая по август 2021 г. За исследуемый период эффективность водоочистки от Cобщ составила 12–32 %, от Cорг – 12–47 %, от Cнеорг – 6–32 % за исключением нескольких месяцев. Так, в январе 2021 г. изменения концентрации Cобщ не произошло, а концентрация Cорг увеличилась на 5 %. В марте 2021 г. концентрация Cнеорг увеличилась на 3 % по сравнению с исходной водой. В целом водоочистка снижает содержание Cорг и Cнеорг в питьевой воде. Однако в период с декабря 2020 по апрель 2021 г. в питьевой воде Cорг преобладает над Cнеорг. Соответственно, в некоторые периоды года вклад в Cобщ определялся разными типами углерода.
Таблица 1. Физико-химические показатели воды за весь период исследований
Table 1. Physicochemical water quality indicators for the entire study period
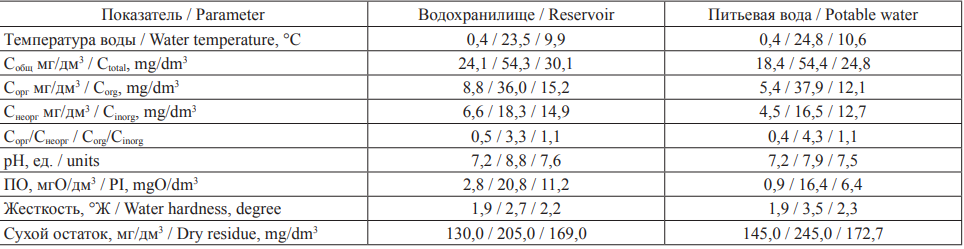
Примечание: ПО – перманганатная окисляемость; количество измерений показателей (n) для водохранилища n = 13 (за исключением ПО: n = 12), для
питьевой воды n = 12.
Notes: PI, permanganate index; the total number of measurements for the Reservoir equals 13 (n = 12 for PI), and that for potable water is 12.
Таблица 2. Физико-химические показатели воды по сезонам (значения представлены в виде М ± m)
Table 2. Physicochemical water quality indicators by season (М ± m)
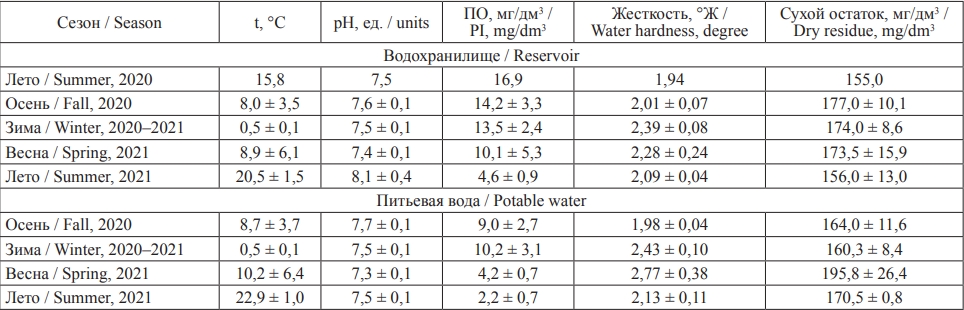
Примечание: ПО – перманганатная окисляемость.
Notes: PI, permanganate index.
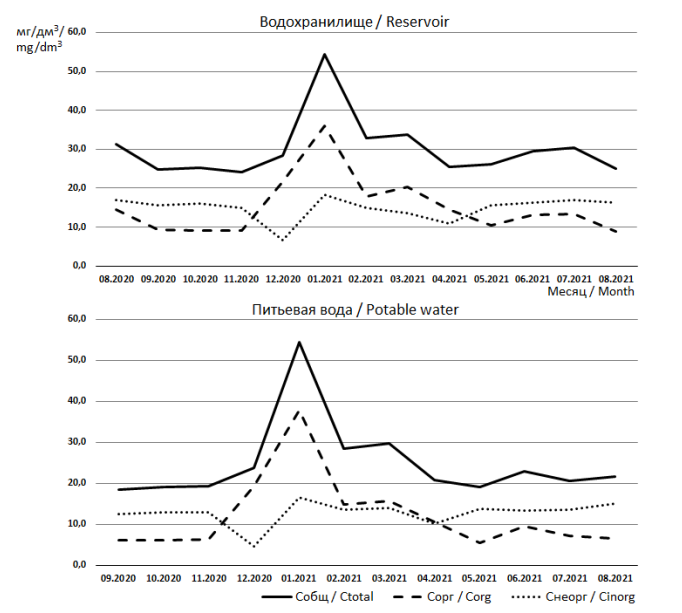
Рисунок. Динамика углерода в водохранилище и питьевой воде
Figure. Changes in carbon concentrations in the Reservoir and potable water
Значения pH воды водохранилища с августа 2021 по апрель 2022 г. находятся в пределах 7,2–7,7 единиц. С мая до августа 2021 г. происходит повышение pH, достигая максимального за весь период значения в августе. В питьевой воде величина pH варьирует в интервале от 7,2 до 7,9 практически без каких-либо сезонных закономерностей; максимальное значение показателя установлено в августе 2020 г. Наибольшие значения ПО в воде водохранилища обнаружены с августа 2020 по апрель 2021 г. с максимальными значениями в октябре и январе. В питьевой воде максимальные значения ПО выявлены в октябре и декабре 2020 г., а с января по август 2021 г. происходило снижение показателя. Водоподготовка обеспечивала снижение ПО в сравнении с исходной природной водой на 28–68 %, за исключением декабря, когда показатель возрос на 44 %.
Максимальные значения жесткости в воде водохранилища выявлены в марте 2021 г., а в питьевой воде – в апреле 2021 г. Наименьшие значения этого показателя обоих видов вод установлены в период с августа по октябрь 2020 г. Наибольшее содержание сухого остатка в воде водохранилища выявлено в марте 2021 г., в питьевой воде – в мае 2021 г. В течение всего периода исследований динамика содержания сухого остатка обоих видов вод не проявляет каких-либо четких тенденций.
Для показателей в воде из водохранилища выявлены следующие значимые корреляции: между Cорг и температурой (R = –0,69; N = 13; p = 0,01), Cорг и Cобщ (R = 0,82; N = 13; p < 0,05), pH и Cнеорг (R = 0,58; N = 13; p = 0,04), ПО и температурой воды (R = –0,66; N = 12; p = 0,02).
Обсуждение. Как известно, количество органического вещества в поверхностных водоемах отражает характер, интенсивность биологических процессов, антропогенное воздействие, а также зависит от физико-географической среды и землепользования в пределах водосборных бассейнов. Повышение концентрации растворенного органического углерода объясняется глобальным изменением климата, например последствиями кислотных осадков или повышения температуры воздуха [11][12]. Ранее нами были установлены очень слабые уровни корреляций между среднегодовой температурой воздуха и концентрациями Cорг в водоемах (r = 0,06…0,42), а также между количеством осадков и Cорг (r = 0,18…0,40) с 2009 по 2019 г. [13]. В исследованиях [14] отмечена сильная зависимость между температурой воздуха и концентрацией растворенного органического углерода в речной воде (США), но в сочетании с сопутствующими гидрологическими условиями, такими как осадки и смыв с берегов в пределах водосборных бассейнов. С учетом результатов текущего исследования можно заключить, что временных интервалов, за которые оценивалась связь между данными климатическими показателями и Cорг, недостаточно, а количество Cоргв воде может подвергаться изменениям, например во время паводка. Повышение подледной концентрации веществ, в частности органического углерода, можно интерпретировать эффектом концентрирования веществ вымораживанием. Как было показано на примере одного из водоемов [15], пространственно концентрации растворенного органического и неорганического углерода в нижележащей водной толще обычно выше, чем в слое льда в холодное время года. Авторами отмечено, что растворенные вещества могут вытесняться из твердой ледяной матрицы и переходить в водную фазу в процессе образования льда. В течение всего срока измеренные концентрации органического углерода в питьевой воде1 были выше установленного нормативного значения 5 мг/дм3 , а при пиковом значении концентрации в зимнее время превышение норматива составило 7,5 раза. Высокие концентрации Cорг питьевой воде создают риски здоровью из-за образования опасных летучих галогенорганических соединений.
Интегральный показатель «перманганатная окисляемость» (ПО) отражает количество легкоокисляемых веществ в воде и служит индикатором органического загрязнения [16]. Обнаруженная отрицательная корреляция между ПО и температурой воды водохранилища не подтверждает предположения о прямой связи температуры и сезонного поступления легкоокисляемых органических соединений в водоеме. Помимо органических соединений, показатель ПО зависит от присутствия железа и марганца в воде [17]. В исследованиях показано [18], что большое значение в динамике показателя имеет эффект накопления – увеличения концентраций ПО при протекании реки через различные населенные пункты и места возможных сбросов. В соответствии с этим годовые и сезонные изменения ПО могут быть следствием различной скорости поступления и накопления некоторых соединений природной и техногенной природы.
В природных водах, помимо небольшого количества свободного СO2 атмосферного происхождения, также содержатся бикарбонат-ионы, находящиеся в равновесии с эквивалентным количеством ионов кальция и магния2 . Немаловажный вклад в обогащение воды неорганическим углеродом вносят хемогенные и биогенные процессы образования и осаждения карбонатов, связанные с сезонностью и глубиной3 , а также минералогический состав донных отложений пресноводных озер [19]. Было показано, что пересыщение воды CO2 происходит преимущественно в водоемах с низкой соленостью и высоким содержанием органического вещества [20]. Содержание свободного СO2 убывает вследствие интенсивно протекающего фотосинтеза и возрастает за счет биохимического разложения органических веществ, а избыточные количества исчезают при соприкосновении воды с атмосферой. В интервале pH от 7,0 до 8,3 содержание гидрокарбонатной формы CO2 находится в пределах 82,7–97,8 % от общего количества CO2 в воде. Начиная с pH 8,0 возрастает доля CO2 в форме карбонатов2 . В условиях слабого поверхностного стока в реку Енисей в некоторые сезоны года установлены малые количества привноса растворенного органического и неорганического углерода [21]. С учетом представленной информации прослеживается связь между содержанием ионов жесткости, изменением pH и увеличением доли Cнеорг. В водохранилище концентрации кальция и магния преобладают в холодное время года. После таяния льда и повышения температуры возрастает биологическая активность воды, а также происходит вовлечение кальция с магнием в хемогенные и биогенные процессы. В свою очередь, преобладание Cнеорг над Cорг в воде водохранилища можно объяснить привносом неорганического углерода в период таяния и дальнейшим увеличением связанного с ионами жесткости CO2 в воде, что возможно при повышенных значениях pH в летнее время. С содержанием в воде гидрокарбонатов, карбонатов, ионов жесткости связан процесс образования и осаждения карбонатных осадков. Отмечено, что в пресноводных озерах Урала донные отложения содержат карбонаты кальция и магния [19]. Исходя из значений концентраций Cнеорг в питьевой воде, процессы водоподготовки не способствуют дополнительному насыщению воды данной формой углерода.
Минерализация воды в первую очередь зависит от количества неорганических минералов и температуры воды2 . Наблюдаемое снижение минерализации в теплое время года, очевидно, происходит вследствие большего растворения веществ и вовлечения их в биогенные процессы. Согласно классификации поверхностных вод Н.И. Толстихина, по выявленным значениям минерализации изучаемое водохранилище можно отнести к нормально пресным водам4 . Содержание растворенного органического вещества и его динамика в основном зависят от двух факторов: происхождения и поступления, а также от его последующей минерализации [22]. Вместе с тем следует различать показатель «общая минерализации воды» и процесс минерализации органического углерода, хотя при определенных гидрохимических условиях между ними существует связь. Повышенная соленость воды и паводки могут вызывать ряд биогеохимических изменений, таких как повышение концентрации сульфатов, увеличение катионного обмена, кислотности и мутности, снижение окислительно-восстановительного потенциала и уровня кислорода, уменьшить запас доступного для микроорганизмов органического субстрата. Но в то же время эти условия могут увеличить пул микробов с высокой способностью к метаболизму углерода [23].
Таким образом, результаты годовых мониторинговых исследований выявили ряд закономерностей показателей физико-химического состава воды. Вместе с тем имеется необходимость оценки глубинных процессов, расширения мониторируемых показателей: БПК, щелочность, комплексообразующая способность, а также разработки алгоритма временного определения показателей для более точной оценки связи с климатическими параметрами.
Выводы
- В период 2020–2021 гг. проведены мониторинговые исследования поверхностного водоисточника и воды после водоочистки по следующим показателям: температуры воды, растворенный углерод, pH, ПО, жесткость, сухой остаток. Пиковые концентрации Cобщ (54,3 мг/дм3 ) и Cорг (36,0 мг/дм3 ) в воде водохранилища были причиной увеличения концентраций углерода в питьевой воде, что несло потенциальный риск для здоровья населения.
- В весенне-летний период 2021 г. значения ПО были значительно ниже, чем в предыдущие сезоны. Значения pH воды водохранилища находились в пределах 7,2–7,7, за исключением лета 2021 г., когда зафиксировано повышение pH; значения показателя в питьевой воде составили 7,2–7,9. Максимальные значения жесткости в природной и питьевой воде выявлены весной 2021 г. По содержанию сухого остатка вода в водохранилище отнесена к категории нормально пресных вод.
- Наибольшее отношение концентраций Cорг/Cнеорг в природной и питьевой воде установлено в период с декабря по апрель. Между Сорг и температурой воды из водохранилища за весь период исследований выявлена отрицательная корреляция, тогда как между pH и Cнеорг корреляция положительная.
- Мероприятия по водоочистке обеспечили снижение Cобщ на 12–32 %, Cорг – на 12–47 %,Cнеорг – на 6–32 %, за исключением января и марта. ПО в питьевой воде снижалась на 28–68 % по сравнению с исходной, за исключением декабря.
1. СанПиН 1.2.3685–21 «Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов среды обитания», утверждены постановлением Главного государственного санитарного врача Российской Федерации от 28 января 2021 года № 2.
2 Унифицированные методы анализа вод. Издание 2-е, исправленное. Под ред. д-ра хим. наук Ю.Ю. Лурье. Москва: изд-во «Химия», 1973. 376 с.
3 Литология. Кн. 2: Учеб. пособие / Фролов В.Т. M.: Изд-во МГУ, 1993. 432 с.
4 Справочник по гидрохимии. Под ред. Никанорова А.М. Л.: Гидрометеоиздат, 1989. 391 с.
Список литературы
1. Konapala G, Mishra AK, Wada Y, Mann ME. Climate change will affect global water availability through compounding changes in seasonal precipitation and evaporation. Nat Commun. 2020;11(1):3044. doi: 10.1038/s41467-020-16757-w
2. Mujere N, Moyce W. Climate change impacts on surface water quality. Ganpat W, Isaac WA, eds. Environmental Sustainability and Climate Change Adaptation Strategies. Hershey, PA: IGI Global; 2017:322-340. doi: 10.4018/978-1-5225-1607-1.ch012
3. Cavicchioli R, Ripple WJ, Timmis KN, et al. Scientists’ warning to humanity: microorganisms and climate change. Nat Rev Microbiol. 2019;17(9):569–586. doi: 10.1038/s41579-019-0222-5
4. Banwart SA, Black H, Cai Z, et al. The global challenge for soil carbon. Banwart SA, Noellemeyer E, Milne E, eds. Soil Carbon: Science, Management and Policy for Multiple Benefits. CAB International; 2015:1-9.
5. Шепоренко Г.А. О тенденции изменения климата Урала. Доступно по: http://svgimet.ru/?page_id=4068 Ссылка активна на 25.08.2022.
6. El-Naggar NA, Moawad MN, Ahmed EF. Toxic phenolic compounds in the Egyptian coastal waters of Alexandria: spatial distribution, source identification, and ecological risk assessment. Water Science. 2022;36(1):32-40. doi: 10.1080/23570008.2022.2031724
7. Adeniji AO, Okoh OO, Okoh AI. Levels of polycyclic aromatic hydrocarbons in the water and sediment of Buffalo River Estuary, South Africa and their health risk assessment. Arch Environ Contam Toxicol. 2019;76(4):657–669. doi: 10.1007/s00244-019-00617-w
8. Саяпин В.В., Сойер В.Г., Милутка М.С., Клещенков А.В. Продукционно-деструкционные процессы и трансформация органического вещества в планктонном сообществе оз. Маныч-Гудило // Труды Южного научного центра Российской академии наук. 2018. T. 7. C. 57–68. doi: 10.23885/1993-6621-2018-7-57-68
9. Хлыстов И.А., Щукина Д.А., Кузьмина Е.А., Плотко Э.Г., Брусницына Л.А. Подходы к нормированию органического углерода и необходимость его обязательного контроля в питьевой воде // Здоровье населения и среда обитания. 2020. T. 9 № 330. C. 61–66. doi: 10.35627/2219-5238/2020-330-9-61-66
10. Gilca AF, Teodosiu C, Fiore S, Musteret CP. Emerging disinfection byproducts: A review on their occurrence and control in drinking water treatment processes. Chemosphere. 2020;259:127476. doi: 10.1016/j.chemosphere.2020.127476
11. Kļaviņš M, Kokorīte I, Rodinovs V. Dissolved organic matter concentration changes in river waters of Latvia. Proceedings of the Latvian Academy of Sciences. Section B. Natural, Exact, and Applied Sciences. 2011;65(1-2):40-47. doi: 10.2478/v10046-011-0017-1
12. Meyer-Jacob C, Michelutti N, Paterson AM, Cumming BF, Keller WB, Smol JP. The browning and re-browning of lakes: Divergent lake-water organic carbon trends linked to acid deposition and climate change. Sci Rep. 2019;9(1):16676. doi: 10.1038/s41598-019-52912-0
13. Хлыстов И.А., Штин Т.Н., Харькова П.К., Замолоцких Т.В., Бугаева А.В., Щукина Д.А. Органическое вещество в поверхностных источниках питьевого водоснабжения г. Екатеринбурга: содержание, идентификация, опасности // Чистая вода России – 2021. Сборник материалов XVI Международного научно-практического симпозиума и выставки. Екатеринбург: ООО «ДжиЛайм», 2021. C. 241–247.
14. Shang P, Lu YH, Du YX, Jaffé R, Findlay RH, Wynn A. Climatic and watershed controls of dissolved organic matter variation in streams across a gradient of agricultural land use. Sci Total Environ. 2018;612:1442-1453. doi: 10.1016/j.scitotenv.2017.08.322
15. Song K, Wen Z, Jacinthe PA, Zhao Y, Du J. Dissolved carbon and CDOM in lake ice and underlying waters along a salinity gradient in shallow lakes of Northeast China. J Hydrol. 2019;571:545-558. doi: 10.1016/j.jhydrol.2019.02.012
16. Laszakovits JR, Kerr A, MacKay AA. Permanganate oxidation of organic contaminants and model compounds. Environ Sci Technol. 2022;56(8):4728-4748. doi: 10.1021/acs.est.1c03621
17. Elsheikh M, Guirguis H, Fathy A. Removal of iron and manganese from groundwater: a study of using potassium permanganate and sedimentation. MATEC Web of Conferences. 2018;162:05018. doi: 10.1051/matecconf/201816205018
18. Chen SS, Kimirei IA, Yu C, Shen Q, Gao Q. Assessment of urban river water pollution with urbanization in East Africa. Environ Sci Pollut Res Int. 2022;29(27):40812–40825. doi: 10.1007/s11356-021-18082-1
19. Шляпников Д.С., Демчук И.Г., Окунев П.В. Минеральные компоненты донных отложений озер Урала. Свердловск: Изд-во Урал. ун-та, 1990. 101 с.
20. Khan H, Laas A, Marcé R, Obrador B. Major effects of alkalinity on the relationship between metabolism and dissolved inorganic carbon dynamics in lakes. Ecosystems. 2020;23:1566–1580. doi: 10.1007/s10021-020-00488-6
21. Prokushkin AS, Korets MA, Panov AV, et al. Carbon and nutrients in the Yenisei River tributaries draining the Western Siberia Peatlands. IOP Conf Ser: Earth Environ Sci. 2019;232:012010. doi: 10.1088/1755-1315/232/1/012010
22. Mostofa KMG, Liu CQ, Mottaleb MA, et al. Dissolved organic matter in natural waters. Mostofa KMG, Yoshioka T, Mottaleb A, Vione D, eds. Photobiogeochemistry of Organic Matter. Principles and Practices in Water Environments. Springer, Berlin, Heidelberg; 2013. doi: 10.1007/978-3-642-32223-5_1
23. Luo M, Huang JF, Zhu WF, Tong C. Impacts of increasing salinity and inundation on rates and pathways of organic carbon mineralization in tidal wetlands: a review. Hydrobiologia. 2019;827:31–49. doi: 10.1007/s10750-017-3416-8
Об авторах
И. А. ХлыстовРоссия
Хлыстов Иван Андреевич – к.б.н., научный сотрудник, исполняющий обязанности заведующего лабораторией гигиены окружающей среды и экологии человека отдела комплексных проблем гигиены и профилактики заболеваний населения
ул. Попова, д. 30, г. Екатеринбург, 620014
П. К. Харькова
Россия
Харькова Полина Константиновна – младший научный сотрудник лаборатории гигиены окружающей среды и экологии человека отдела комплексных проблем гигиены и профилактики заболеваний населения
ул. Попова, д. 30, г. Екатеринбург, 620014
А. В. Бугаева
Россия
Бугаева Александра Владиславовна – младший научный сотрудник лаборатории гигиены окружающей среды и экологии человека отдела комплексных проблем гигиены и профилактики заболеваний населения
ул. Попова, д. 30, г. Екатеринбург, 620014
Т. В. Замолоцких
Россия
Замолоцких Татьяна Викторовна – научный сотрудник лаборатории гигиены окружающей среды и экологии человека отдела комплексных проблем гигиены и профилактики заболеваний населения
ул. Попова, д. 30, г. Екатеринбург, 620014
Т. Н. Штин
Россия
Штин Татьяна Николаевна – заведующий отделом физико-химических методов исследования
ул. Попова, д. 30, г. Екатеринбург, 620014
В. Б. Гурвич
Россия
Гурвич Владимир Борисович – д.м.н., научный руководитель
ул. Попова, д. 30, г. Екатеринбург, 620014
Рецензия
Для цитирования:
Хлыстов И.А., Харькова П.К., Бугаева А.В., Замолоцких Т.В., Штин Т.Н., Гурвич В.Б. Определение индикативных показателей для организации мониторинга источников питьевого водоснабжения при изменении климатических условий. Здоровье населения и среда обитания – ЗНиСО. 2022;(9):84-90. https://doi.org/10.35627/2219-5238/2022-30-9-84-90
For citation:
Khlystov I.A., Kharkova P.K., Bugaeva A.V., Zamolotskikh T.V., Shtin T.N., Gurvich V.B. Determination of Key Quality Indicators for Organization of Potable Water Source Monitoring under Changing Climatic Conditions. Public Health and Life Environment – PH&LE. 2022;(9):84-90. (In Russ.) https://doi.org/10.35627/2219-5238/2022-30-9-84-90









.png)



























