Перейти к:
Оценка влияния на биоэнергетические процессы клеток наночастиц селена как фактора химического риска производственной и окружающей среды для здоровья
https://doi.org/10.35627/2219-5238/2022-30-9-29-34
Аннотация
Введение. Высокие объемы добычи селена и широкое применение его соединений связано с потенциальными рисками для здоровья человека. В частности, некоторые производственные процессы медеплавильной промышленности являются источниками поступления селенсодержащих наночастиц в окружающую среду.
Цель исследования: оценить токсическое действие наночастиц оксида селена как фактора химического риска производственной и окружающей среды для здоровья.
Материалы и методы. Наночастицы оксида селена (НЧ SeO) были получены методом лазерной абляции. Исследования по оценке токсичности НЧ SeO проводились: in vitro – на клеточной культуре ФЛЭЧ-104 с анализом биолюминесценции АТФ и определением скорости потребления кислорода; in vivo – на белых аутбредных крысах с оценкой ультраструктурных изменений тканей методом электронной микроскопии, измерением активности СДГ лимфоцитов и метаболомным анализом крови.
Результаты. В эксперименте in vitro было показано снижение биолюминесценции АТФ (на 75,9 % при концентрации НЧ SeO 100 мкг/мл в инкубационной среде) и скорости потребления кислорода (на 79,8 % при концентрации НЧ SeO 100 мкг/мл в инкубационной среде). Активность СДГ лимфоцитов крови в эксперименте in vivo снижалась с увеличением дозы (на 10,12; 14,0; 15,9 % в сравнении с контролем соответственно группам «НЧ SeO 0,1», «НЧ SeO 0,5», «НЧ SeO 1»). Исследование ультраструктурных изменений клеток ткани печени показало меньшее количество нормальных митохондрий в сравнении с контролем (на 7,78 % в группе «НЧ SeO 1»), метаболомный анализ выявил уменьшение содержания ацилкарнитинов и увеличение лизофосфатидилинозитолов (p > 0,05).
Выводы. В результате проведенных экспериментальных исследований как in vitro, так и in vivo была установлена способность НЧ SeO оказывать негативное воздействие на биоэнергетические процессы в клетке, включающее как минимум два механизма: нарушение внутримитохондриального β-окисления жирных кислот и инактивацию сукцинатдегидрогеназы. Фундаментальная роль последней в цепи переноса электронов митохондрий делает ее жизненно важной для большинства многоклеточных организмов. Полученные результаты могут быть использованы в качестве научной основы для оценки селенсодержащих наночастиц как фактора химического риска производственной и окружающей среды для здоровья и поиска подходов к управлению такими рисками.
Ключевые слова
Для цитирования:
Рябова Ю.В., Сутункова М.П., Чемезов А.И., Минигалиева И.А., Бушуева Т.В., Шеломенцев И.Г., Клинова С.В. Оценка влияния на биоэнергетические процессы клеток наночастиц селена как фактора химического риска производственной и окружающей среды для здоровья. Здоровье населения и среда обитания – ЗНиСО. 2022;(9):29-34. https://doi.org/10.35627/2219-5238/2022-30-9-29-34
For citation:
Ryabova Yu.V., Sutunkova M.P., Chemezov A.I., Minigalieva I.A., Bushueva T.V., Shelomentsev I.G., Klinova S.V. Evaluation of Effects of Selenium Nanoparticles as an Occupational and Environmental Chemical Hazard on Cellular Bioenergetic Processes. Public Health and Life Environment – PH&LE. 2022;(9):29-34. (In Russ.) https://doi.org/10.35627/2219-5238/2022-30-9-29-34
Введение. С высокими объемами добычи селена [1] и широким применением связаны потенциальные риски для здоровья человека. Некоторые производственные процессы медеплавильной промышленности являются источниками поступления селенсодержащих наночастиц в воздух рабочей зоны и окружающую среду. К ним относятся переработка медных шламов, обжиг медного колчедана, производство марганца, селена и теллура. Более того, контакт с селенсодержащими наночастицами возможен в стекольном производстве, производстве керамики, в резиновой и химической промышленности и не ограничивается производственной деятельностью.
Помимо производственно-обусловленного действия селенсодержащих наночастиц (НЧ), вызывает опасение целенаправленное их применение. В современной литературе широко распространены данные о положительных свойствах селенсодержащих НЧ – антибактериальных [2][3], противоопухолевых [2–6], антиоксидантных [7]. Ряд исследователей указывают на необходимость применения селенсодержащих НЧ в сочетании с противоопухолевыми средствами, поскольку это не только позволяет несколько ослабить токсическое воздействие химиотерапевтических препаратов [4][8], но и усиливает эффекты противоопухолевой терапии [4]. В определенных дозах их рассматривают в качестве потенциального лекарственного средства для лечения нейродегенеративных заболеваний, таких как болезнь Альцгеймера [9].
Притом что чаще учитывается их положительное действие, но не токсическое, в современной литературе имеются единичные данные о токсических эффектах селенсодержащих НЧ на клеточном и органо-системном уровне, которые, однако, изучены недостаточно и в небольшом числе экспериментальных исследований с несколько противоречивыми результатами [например, 10–13].
Целью работы являлась оценка влияния на биоэнергетические процессы клеток наночастиц селена как фактора химического риска производственной и окружающей среды для здоровья.
Материалы и методы. Исследования по оценке токсического действия селенсодержащих НЧ были выполнены на примере наночастиц оксида селена (НЧ SeO). Суспензия, содержащая НЧ SeO (форма, приближенная к сферической; средний диаметр использованных частиц 51 ± 14 нм; дзета-потенциал до 42 mV) была получена методом лазерной абляции тонких листовых мишеней из селена 99,99 % чистоты под слоем стерильной деионизированной воды в ЦКП «Современные нанотехнологии» УрФУ.
Оценка действия НЧ SeO in vitro выполнялась на культуре фибробластоподобных клеток линии ФЛЭЧ-104 ООО «БиолоТ» (Санкт-Петербург, Россия). Клетки высевали в 96-луночный планшет и инкубировали в стандартных условиях в течение 48 ч до получения монослоя. Затем в лунки добавляли суспензию НЧ SeO (концентрация НЧ в среде составляла 25, 50 либо 100 мкг/мл) и инкубировали в течение 24 ч в стандартных условиях. Для количественной оценки цитотоксических эффектов применялся анализ биолюминесценции АТФ. Результаты измерений были представлены в относительных единицах люминесценции (RLU). Скорость потребления кислорода клеток определяли с помощью клеточного анализатора метаболизма.
Оценка действия НЧ SeO in vivo была проведена на аутбредных белых крысах-самцах возрастом около 4 месяцев на начало эксперимента по 12 животных в каждой группе. Начальная масса тела животных составляла 200–270 г, диапазон колебания массы животных не превышал ±20 % от средней массы. Субхроническая интоксикация моделировалась путем повторных внутрибрюшинных инъекций 3 раза в неделю в течение 6 недель (всего 18 введений). Выбор доз был проведен на основании результатов ранее проведенных экспериментальных исследований. Вводились растворы стабильной суспензии НЧ объемом 1 мл в разовой дозе 0,2 мг/кг и 1 мл деионизированной воды (группа «НЧ SeO 0,1»); объемом 2 мл суспензии НЧ в разовой дозе 1 мг/кг (группа «НЧ SeO 0,5»); объемом 2 мл суспензии НЧ в разовой дозе 2 мг/кг (группа «НЧ SeO 1»); 2 мл деионизированной воды («Контроль»).
Содержание, питание, уход за животными и выведение их из эксперимента осуществляли в соответствии с общепринятыми требованиями. Работа одобрена Локальным этическим комитетом ФБУН ЕМНЦ ПОЗРПП, номер протокола № 2 от 20.04.2021.
В качестве показателей состояния биоэнергетического обмена использовали определение активности сукцинатдегидрогеназы (СДГ) лимфоцитов крови [14].
Метаболомный скрининг проводился с использованием ВЭЖХ-МС. Детектирование осуществляли времяпролетным масс-спектрометром. Полученный массив данных по всем пробам обрабатывали в программном обеспечении, позволяющем выделить статистически значимые изменения содержания метаболитов посредством обработки данных методом главных компонент. Для каждой экспериментальной группы был получен набор значений m/z, статистически значимо изменивших интенсивность в сравнении до и после проведения эксперимента. Для данных масс проводили аннотацию посредством повторного анализа на масс-спектрометре в тандемном режиме с разными уровнями энергий фрагментации для получения характеристических фрагментных спектров и расшифровки структуры. Анализ полученных спектров проводили с использованием общедоступных баз данных (HMDB, MoNA, METLIN, MassBank EU), а также in silico инструментов фрагментации (MetFrag, CFM‑ID, MS-FINDER).
Ультраструктура клеток оценивалась с использованием электронного микроскопа в режиме STEM. Степень повреждения митохондрий определялась по классификации Mei G. Sun исходя из морфологических характеристик (матриксное пространство, количество крист) [15]. К нормальным относили митохондрии типа А (нормальные) и В (нормально-везикулярные), в то время как типы C (везикулярные), D (везикулярно-вздутые), E (вздутые) считали патологически-измененными.
Статистическая значимость межгрупповых различий средних значений всех полученных показателей оценивалась с помощью t-критерия Стьюдента с поправкой на множественные сравнения. Различия считались статистически значимыми при уровне случайности р < 0,05.
Результаты
Цитотоксичность. В эксперименте in vitro на клеточной линии ФЛЭЧ-104 были получены зависимости АТФ-зависимой люминесценции и скорости потребления кислорода (рис. 1) при воздействии разных концентраций НЧ SeO в инкубационной среде.

Рис. 1. Изменение в культуре клеток при воздействии разных концентраций НЧ SeO в инкубационной среде:
А – АТФ-зависимая люминесценция (RLU); B – скорость потребления кислорода клеточной линией.
По оси абсцисс отложены действующие концентрации наночастиц в инкубационной среде, мкг/мл;
по ординате отложены значения показателя в культуре клеток.
Примечание: * – значения, имеющие статистически значимые отличия от контрольной группы (по t-критерию Стьюдента
при p ≤ 0,05).
Fig. 1. Changes in the cell culture under effect of various concentrations of SeO NPs in the incubation medium:
A – ATP bioluminescence (RLU), B – oxygen consumption rates of FLEH-104 cells. The x-axis shows concentrations
of nanoparticles in the incubation medium in μg/mL, and the y-axis shows the values established in the cell culture.
Note: * – statistically different from the control group (Student’s t-test, p ≤ 0.05).
Ультраструктурные изменения клеток тканей печени. Процентное соотношение нормальных митохондрий типа А и В по Mei G. Sun составило 87,44 ± 1,14 % в группе «НЧ SeO 1», 94,82 ± 0,95 % в группе «Контроль» при p < 0,05.
Активность сукцинатдегидрогеназы. Результаты измерения активности сукцинатдегидрогеназы в лимфоцитах крови (число гранул формазана в 50 лимфоцитах) представлены на рис. 2.
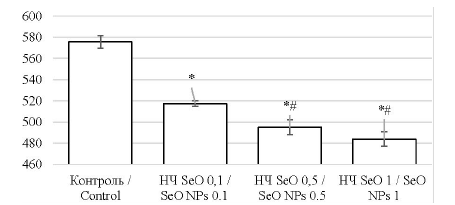
Рис. 2. Активность сукцинатдегидрогеназы (СДГ) в лимфоцитах крови: по оси абсцисс указаны группы животных;
по оси ординат отложены значения активности СДГ (число гранул формазана в 50 лимфоцитах)
Примечание: * – значения, имеющие статистически значимые отличия от контрольной группы; # – от группы
«НЧ SeO 0,1» (по t-критерию Стьюдента при p ≤ 0,05).
Fig. 2. SDH activity in blood lymphocytes: the x-axis shows experimental groups of animals; the y-axis shows SDH activity
values (the number of formazan granules per 50 lymphocytes)
Notes: * statistically different from the control group; # statistically different from the SeO NPs 0.1 group (Student’s t-test, p ≤ 0.05).
Метаболомные исследования. Общее количество метаболитов, идентифицированные метаболиты и изменения их содержания в крови экспериментальных животных представлены в таблице.
Обсуждение. При оценке цитотоксичности НЧ SeO в эксперименте in vitro на клеточной линии ФЛЭЧ-104 было установлено, что токсичность этих наночастиц бывает различной в зависимости от воздействия разных концентраций НЧ SeO в инкубационной среде. Так, НЧ SeO вызывают снижение интенсивности АТФ-зависимой люминесценции, что может говорить о замедлении процессов жизнедеятельности и снижении энергетического потенциала клеток, оцененное на всех исследованных нами концентрациях НЧ SeO в инкубационной среде (рис. 1А). Кроме того, снижалась скорость потребления кислорода митохондриями (рис. 1B).
Изменение параметров, прямо или косвенно говорящих о нарушении функции митохондрий, было установлено и в эксперименте in vivo по изучению токсического действия НЧ SeO на организм животных. При ультраструктурном исследовании методом электронной микроскопии отмечено снижение процентного соотношения нормальных митохондрий в тканях печени. Нарушение ультраструктуры митохондрий приводило к снижению их энергетического потенциала, о котором косвенно судили по статистически значимому, монотонному и дозозависимому снижению активности сукцинатдегидрогиназы под воздействием НЧ SeO (рис. 2). Снижение активности СДГ, вероятно, связано с известной из литературы способностью селена замещать серу в соединениях [16].
Нарушение функций митохондрий подтверждается результатами метаболомного скрининга. Так, было найдено статистически значимое увеличение содержания лизофосфатидилинозитолов [17] в группах НЧ SeO 0,1 и НЧ SeO 1. Лизофосфатидилинозитолы выступают как прекурсоры для синтеза фосфатидилинозитолдии трифосфатов – модификаторов мембран, изменяющих их текучесть и, таким образом, способствующих изменению активности мембранных каналов [18]. Также известно, что процессы спайки и расщепления фосфолипидных мембран, в т. ч. митохондрий, связаны с обогащением последних производными LPI [19]. Кроме того,данные вещества являются лигандами для GPR55 [20] – рецептора, сопряженного с G-белком, опосредующим внутриклеточные сигнальные каскады. Совокупность эффектов, проявляемых парой LPI-GPR55 [19][21–23], может соотноситься с интенсификацией процессов энергетического обмена и регенерации организма в ответ на повреждения, вызванные НЧ SeO. Изменение содержания лизофосфатидилинозитолов в работах по изучению метаболомного отклика организма на действие соединений селена даже в солевой форме ранее выявлено не было.
Таблица. Результаты метаболомного анализа крови крыс, подвергшихся субхроническому воздействию наночастиц SeO
Table. Results of the blood-based metabolomic test of rats following a subchronic exposure to SeO nanoparticles

Примечание: LPI – лизофосфатидилинозитол. Символом «↑» обозначается повышение интенсивности аналитического сигнала массы метаболита при
сравнении до и после эксперимента: символом «↓» – снижение; «–» – для данного вещества не выявлено значимого изменения содержания в данной
группе.
Notes: LPI, lysophosphatidylinositole. The arrows ↑ and ↓ indicate an increase/decrease in the signal intensity for the mass of the metabolite after the experiment,
and the dash means that no significant change in the signal intensity was observed.
Во всех опытных группах повышается содержание ацилкарнитинов и их производных согласованно и пропорционально общим изменениям количеств веществ в крови. Данные метаболиты, с одной стороны, переносят жирные кислоты через карнитиновый челнок во внутренних мембранах митохондрий для дальнейшего бета-окисления, с другой – транспортируют излишки продуктов данного процесса из митохондрий и далее во внеклеточное пространство, поскольку избыток оксиацил-КоА производных нарушает функции митохондрий вплоть до инициации апоптоза [24–26]. Вариации в содержании данных веществ свидетельствуют об изменениях в процессе бета-окисления жирных кислот, происходящего в митохондриях, что было показано ранее для воздействия солевых форм селена [27] и впервые показано нами для его воздействия в форме НЧ.
Заключение. Наночастицы оксида селена способны угнетать биоэнергетические процессы в клетке, что мы продемонстрировали как в экспериментах in vitro (снижение интенсивности АТФ-зависимой люминесценции на фибробластоподобных клетках линии ФЛЭЧ-104), так и в исследованиях in vivo (снижение активности сукцинатдегидрогеназы у беспородных белых крыс).
Негативное влияние на энергетическую функцию митохондрий реализуется, по всей видимости, за счет как минимум двух механизмов: нарушения внутримитохондриального β-окисления жирных кислот и инактивации сукцинатдегидрогеназы, чья фундаментальная роль в цепи переноса электронов митохондрий делает ее жизненно важной для большинства многоклеточных организмов.
Такие нарушения обуславливают снижение процентного соотношения нормальных митохондрий в клетках, в первую очередь, печени, являющейся органом-мишенью для воздействия селена.
Полученные в исследованиях in vitro и in vivo результаты могут быть использованы в качестве научной основы для оценки селенсодержащих НЧ как фактора химического риска производственной и окружающей среды для здоровья и поиска подходов к управлению такими рисками. Кроме того, упомянутые изменения могут служить отправной точкой для поиска предикторов ранней диагностики нарушений, опосредованных воздействием селенсодержащих НЧ.
Список литературы
1. Кульчицкий Н.А., Наумов А.В. Современное состояние рынков селена и соединений на его основе. Известия вузов. Цветная металлургия. 2015. № 3. С. 40–48. doi: 10.17073/0021-3438-2015-3-40-48
2. Geoffrion LD, Hesabizadeh T, Medina-Cruz D, et al. Naked selenium nanoparticles for antibacterial and anticancer treatments. ACS Omega. 2020;5(6):2660-2669. doi: 10.1021/acsomega.9b03172
3. Keyhani A, Shakibaie M, Mahmoudvand H, et al. Prophylactic activity of biogenic selenium nanoparticles against chronic Toxoplasma gondii infection. Recent Pat Antiinfect Drug Discov. 2020;15(1):75-84. doi: 10.2174/1574891X15666200604115001
4. Gao F, Yuan Q, Gao L, et al. Cytotoxicity and therapeutic effect of irinotecan combined with selenium nanoparticles. Biomaterials. 2014;35(31):8854-8866. doi: 10.1016/j.biomaterials.2014.07.004
5. Sonkusre P. Specificity of biogenic selenium nanoparticles for prostate cancer therapy with reduced risk of toxicity: an in vitro and in vivo study. Front Oncol. 2020;9:1541. doi: 10.3389/fonc.2019.01541
6. Jin Y, Cai L, Yang Q, et al. Anti-leukemia activities of selenium nanoparticles embedded in nanotube consisted of triple-helix β-d-glucan. Carbohydr Polym. 2020;240:116329. doi: 10.1016/j.carbpol.2020.116329
7. Dehkordi AJ, Mohebbi AN, Aslani MR, Ghoreyshi SM. Evaluation of nanoselenium (Nano-Se) effect on hematological and serum biochemical parameters of rat in experimentally lead poisoning. Hum Exp Toxicol. 2017;36(4):421-427. doi: 10.1177/0960327116651124
8. Rezvanfar MA, Rezvanfar MA, Shahverdi AR, et al. Protection of cisplatin-induced spermatotoxicity, DNA damage and chromatin abnormality by selenium nano-particles. Toxicol Appl Pharmacol. 2013;266(3):356-365. doi: 10.1016/j.taap.2012.11.025
9. Sun J, Wei C, Liu Y, et al. Progressive release of mesoporous nano-selenium delivery system for the multi-channel synergistic treatment of Alzheimer’s disease. Biomaterials. 2019;197:417-431. doi: 10.1016/j.biomaterials.2018.12.027
10. Hadrup N, Loeschner K, Skov K, et al. Effects of 14-day oral low dose selenium nanoparticles and selenite in rat – as determined by metabolite pattern determination. Peer J. 2016;4:e2601. doi: 10.7717/peerj.2601
11. He Y, Chen S, Liu Z, Cheng C, Li H, Wang M. Toxicity of selenium nanoparticles in male Sprague-Daley rats at supranutritional and nonlethal levels. Life Sci. 2014;115(1-2):44-51. doi: 10.1016/j.lfs.2014.08.023
12. Lesnichaya M, Shendrik R, Titov E, Sukhov B. Synthesis and comparative assessment of antiradical activity, toxicity, and biodistribution of κ-carrageenan-capped selenium nanoparticles of different size: in vivo and in vitro study. IET nanobiotechnol. 2020;14(6):519–526. doi: 10.1049/iet-nbt.2020.0023
13. Urbankova L, Skalickova S, Pribilova M, et al. Effects of sub-lethal doses of selenium nanoparticles on the health status of rats. Toxics. 2021;9(2):28. doi: 10.3390/toxics9020028
14. Нарциссов Р.П. Применение n-нитротетразоли фиолетового для количественной цитохимии дегидрогеназ лимфоцитов человека. Архив анатомии, гистологии и эмбриологии. 1969. Т. 56. № 5. С. 85–91.
15. Sun MG, Williams J, Munoz-Pinedo C, et al. Correlated three-dimensional light and electron microscopy reveals transformation of mitochondria during apoptosis. Nat Cell Biol. 2007;9(9):1057-1065. doi: 10.1038/ncb1630
16. Yücel UM, Başbuğan Y, Uyar A, Kömüroğlu AU, Keleş ÖF. Use of an antiarrhythmic drug against acute selenium toxicity. J Trace Elem Med Biol. 2020;59:126471. doi: 10.1016/j.jtemb.2020.126471
17. Darnell JC, Osterman DG, Saltiel AR. Synthesis of phosphatidylinositol in rat liver microsomes is accompanied by the rapid formation of lysophosphatidylinositol. Biochim Biophys Acta. 1991;1084(3):269–278. doi: 10.1016/0005-2760(91)90069-t
18. Poccia D, Larijani B. Phosphatidylinositol metabolism and membrane fusion. Biochem J. 2009;418(2):233–246. doi: 10.1042/bj20082105
19. Piñeiro R, Falasca M. Lysophosphatidylinositol signalling: New wine from an old bottle. Biochim Biophys Acta. 2012;1821(4):694-705. doi: 10.1016/j.bbalip.2012.01.009
20. Arifin SA, Falasca M. Lysophosphatidylinositol signalling and metabolic diseases. Metabolites. 2016;6(1):6. doi: 10.3390/metabo6010006
21. Makide K, Uwamizu A, Shinjo Y, et al. Novel lysophosphoplipid receptors: their structure and function. J Lipid Res. 2014;55(10):1986-1995. doi: 10.1194/jlr.R046920
22. Fondevila MF, Fernandez U, Gonzalez-Rellan MJ, et al. The L-α-lysophosphatidylinositol/G protein-coupled receptor 55 system induces the development of nonalcoholic steatosis and steatohepatitis. Hepatology. 2021;73(2):606-624. doi: 10.1002/hep.31290
23. Calvillo-Robledo A, Cervantes-Villagrana RD, Morales P, Marichal-Cancino BA. The oncogenic lysophosphatidylinositol (LPI)/GPR55 signaling. Life Sci. 2022;301:120596. doi: 10.1016/j.lfs.2022.120596
24. Wojtczak L. Effect of long-chain fatty acids and acyl-CoA on mitochondrial permeability, transport, and energy-coupling processes. J Bioenerg Biomembr. 1976;8(6):293–311. doi: 10.1007/BF00765158
25. Su X, Han X, Mancuso DJ, Abendschein DR, Gross RW. Accumulation of long-chain acylcarnitine and 3-hydroxy acylcarnitine molecular species in diabetic myocardium: identification of alterations in mitochondrial fatty acid processing in diabetic myocardium by shotgun lipidomics. Biochemistry. 2005;44(13):5234-5245. doi: 10.1021/bi047773a
26. Violante S, Ijlst L, te Brinke H, et al. Carnitine palmitoyltransferase 2 and carnitine/acylcarnitine translocase are involved in the mitochondrial synthesis and export of acylcarnitines. FASEB J. 2013;27(5):2039–2044. doi: 10.1096/fj.12-216689
27. Fernandes J, Hu X, Smith MR, Go YM, Jones DP. Selenium at the redox interface of the genome, metabolome and exposome. Free Radic Biol Med. 2018;127:215-227. doi: 10.1016/j.freeradbiomed.2018.06.002
Об авторах
Ю. В. РябоваРоссия
Рябова Юлия Владимировна – младший научный сотрудник отдела токсикологии и биопрофилактики
ул. Попова, д. 30, г. Екатеринбург, 620014
М. П. Сутункова
Россия
Сутункова Марина Петровна – д.м.н., директор
ул. Попова, д. 30, г. Екатеринбург, 620014
А. И. Чемезов
Россия
Чемезов Алексей Игоревич – научный сотрудник отдела молекулярной биологии и электронной микроскопии
ул. Попова, д. 30, г. Екатеринбург, 620014
И. А. Минигалиева
Россия
Минигалиева Ильзира Амировна – д.б.н., заведующий отделом токсикологии и биопрофилактики
ул. Попова, д. 30, г. Екатеринбург, 620014
Т. В. Бушуева
Россия
Бушуева Татьяна Викторовна – к.м.н., заведующий НПО лабораторно-диагностических технологий
ул. Попова, д. 30, г. Екатеринбург, 620014
И. Г. Шеломенцев
Россия
Шеломенцев Иван Глебович – научный сотрудник отдела молекулярной биологии и электронной микроскопии
ул. Попова, д. 30, г. Екатеринбург, 620014
С. В. Клинова
Россия
Клинова Светлана Владиславовна – научный сотрудник отдела токсикологии и биопрофилактики
ул. Попова, д. 30, г. Екатеринбург, 620014
Рецензия
Для цитирования:
Рябова Ю.В., Сутункова М.П., Чемезов А.И., Минигалиева И.А., Бушуева Т.В., Шеломенцев И.Г., Клинова С.В. Оценка влияния на биоэнергетические процессы клеток наночастиц селена как фактора химического риска производственной и окружающей среды для здоровья. Здоровье населения и среда обитания – ЗНиСО. 2022;(9):29-34. https://doi.org/10.35627/2219-5238/2022-30-9-29-34
For citation:
Ryabova Yu.V., Sutunkova M.P., Chemezov A.I., Minigalieva I.A., Bushueva T.V., Shelomentsev I.G., Klinova S.V. Evaluation of Effects of Selenium Nanoparticles as an Occupational and Environmental Chemical Hazard on Cellular Bioenergetic Processes. Public Health and Life Environment – PH&LE. 2022;(9):29-34. (In Russ.) https://doi.org/10.35627/2219-5238/2022-30-9-29-34









.png)



























