Перейти к:
Этиология внебольничных пневмоний в период эпидемического распространения Covid-19 и оценка риска возникновения пневмоний, связанных с оказанием медицинской помощи
https://doi.org/10.35627/2219-5238/2021-29-7-67-75
Аннотация
Введение. Пандемия COVID-19 в 2020 году внесла свой вклад в эпидемиологию респираторных инфекций. Важным является своевременное проведение дифференциальной диагностики COVID-19 и сезонных острых респираторных заболеваний. У пациентов с новой коронавирусной инфекцией возрастает риск развития госпитальной пневмонии. Актуальным является анализ особенностей циркуляции резистентных к антибактериальным химиопрепаратам штаммов возбудителей внутрибольничных инфекций.
Цель – изучение этиологической структуры внебольничных пневмоний в период эпидемического распространения COVID-19 и оценка рисков возникновения пневмоний, связанных с оказанием медицинской помощи.
Материалы и методы. Исследовали биологический материал от 446 пациентов с диагнозом «внебольничная пневмония», находившихся на амбулаторном лечении или в стационарах г. Ростова-на-Дону. Верификация респираторных вирусов, включая РНК SARS-CoV-2, а также M. pneumoniae, C. pneumoniae, L. pneumophila выполнена методом полимеразной цепной реакции в мазках носоглотки. Бактериологический анализ мокроты проводили с использованием дифференциально-диагностических сред, идентификацию выделенных патогенов осуществляли с помощью времяпролетной масс-спектрометрии на приборе Autoflex (Bruker Daltonics) c программным обеспечением BioTyper 3,0.
Результаты и обсуждение. В период распространения новой коронавирусной инфекции в Ростовской области доля положительных результатов на SARS-CoV-2 среди пациентов с диагнозом «внебольничная пневмония» составляет 35,6 %. Частота микст-инфекций вирусной природы достоверно не отличалась среди пациентов с лабораторно подтвержденным диагнозом COVID-19 и пациентов с отрицательным результатом на SARS-CoV-2 (25,9 и 26,2 % соответственно). В структуре микробиоты пневмоний, не обусловленных SARS-CoV-2, превалировали грибы рода Candida и плазмокоагулирущие стафилококки. Достоверно чаще от пациентов с лабораторно подтвержденным COVID-19 изолировали культуры неферментирующих грамотрицательных бактерий. У 51,6 % пациентов, проходивших лечение в стационаре, отмечено вторичное коинфицирование, вероятно, связанное с объектами внешней среды или с передачей инфекции от персонала. Передача ИСМП между пациентами не установлена.
Ключевые слова
Для цитирования:
Попова А.Ю., Ежлова Е.Б., Демина Ю.В., Носков А.К., Ковалев Е.В., Карпущенко Г.В., Чемисова О.С., Пичурина Н.Л., Павлович Н.В., Водопьянов С.О., Гудуева Е.Н., Слись С.С., Пшеничная Н.Ю., Литовко А.Р., Асмолова Н.Ю. Этиология внебольничных пневмоний в период эпидемического распространения Covid-19 и оценка риска возникновения пневмоний, связанных с оказанием медицинской помощи. Здоровье населения и среда обитания – ЗНиСО. 2021;(7):67-75. https://doi.org/10.35627/2219-5238/2021-29-7-67-75
For citation:
Popova A.Yu., Ezhlova E.B., Demina Yu.V., Noskov A.K., Kovalev E.V., Karpushchenko G.V., Chemisova O.S., Pichurina N.L., Pavlovich N.V., Vodopyanov S.O., Gudueva E.N., Slis S.S., Pshenichnaya N.Yu., Litovko A.R., Asmolova N.Yu. Etiology of Community-Acquired Pneumonia during the Epidemic Spread of COVID-19 and Healthcare-Associated Pneumonia Risk Assessment. Public Health and Life Environment – PH&LE. 2021;(7):67-75. (In Russ.) https://doi.org/10.35627/2219-5238/2021-29-7-67-75
Введение. В последние годы острые респираторные инфекции верхних отделов дыхательных путей (ОРИВДП) занимают более 90 % от числа всех инфекционных и паразитарных болезней, регистрируемых в Российской Федерации. Проблема высокой заболеваемости ОРИВДП осложняется присоединением вторичной бактериальной коинфекции и развитием внебольничных пневмоний (ВП). Среднемноголетняя заболеваемость внебольничными пневмониями (ВП) в Российской Федерации составила 401,7 на 100 000 населения (2014–2018 гг.). При обследовании превалируют Streptococcus pneumoniae, Haemophilus influenzae, против которых проводится иммунизация в рамках национального календаря профилактических прививок, а также Mycoplasma pneumoniae1 [1].
Пандемия COVID-19, вызванная новой разновидностью коронавируса SARS-CoV-2 в 2020 году, внесла свой вклад в эпидемиологию респираторных инфекций [2]. Важным является своевременное проведение дифференциальной диагностики COVID-19, сезонных острых респираторных вирусных инфекций (ОРВИ), гриппа и ОРИВДП бактериальной этиологии. Внимание медицинских работников направлено на изучение проблемы совместного инфицирования пациентов COVID-19 с другими респираторными вирусами. По данным разных авторов, распространенность сопутствующей и вторичной инфекции, ассоциированной с COVID-19, может составлять от 0,6 до 45,0 %, наиболее распространенными вирусными коинфекциями были риновирусы/ энтеровирусы и грипп А, а также сезонные коронавирусы, респираторно-синцитиальный вирус, вирусы парагриппа, метапневмовирус и вирус гриппа В. Кроме того, у пациентов COVID-19, коинфицированных вирусом гриппа А, были зарегистрированы ложноотрицательные результаты ПЦР на SARS-CoV-2 [3–7].
Для респираторных вирусов характерна способность нарушать регуляцию как врожденного, так и приобретенного иммунитета, что приводит к развитию бактерий в обычно стерильных участках дыхательных путей. Повреждение вирусами эпителия, разрушение легочного сурфактанта и отслаивание клеток в дыхательные пути обеспечивают доступ и богатый источник питательных веществ, способствуя быстрому росту бактерий [8]. При изучении тяжелых или смертельных случаев во время пандемии вируса гриппа A(H1N1)pdm2009 в 2009 году было обнаружено, что бактериальная пневмония осложняла от одной четверти до половины случаев болезни, наиболее распространенными этиологическими агентами вторичной бактериальной пневмонии были S. pneumoniae и Staphylococcus aureus [9–11]. При COVID-19 ранее исследователями выявлены бактериальные патогены S. pneumoniae, Klebsiella pneumoniae, Acinetobacter baumannii, Staphylococcus aureus, M. pneumoniae, L. pneumophila, Aspergillus flavus, Candida spp. [5][12]. Вместе с тем необходимо отметить, что, помимо риска развития внебольничной пневмонии у пациентов с новой коронавирусной инфекцией за счет синергизма вируса и бактерий, серьезную угрозу представляет и развитие у пациентов госпитальной инфекции. Более 90 % госпитализированных больных с диагнозом «пневмония» связаны с искусственной вентиляцией легких в отделениях интенсивной терапии. Неудивительно, что бактериальные коинфекции были зарегистрированы у пациентов с ближневосточным респираторным синдромом (БВРС-КоВ), получавших интенсивную терапию [13–15]. Риск развития госпитальной пневмонии значительно возрастает по мере увеличения срока госпитализации. Как правило, при внутрибольничной пневмонии наблюдается множественная лекарственная устойчивость возбудителей, что ухудшает прогноз исхода заболевания. При выборочном исследовании 1495 пациентов с COVID-19 в больнице г. Ухани 6,8 % пациентов имели вторичные бактериальные инфекции, и почти половина из них (49,0 %) умерли во время госпитализации. В тройку наиболее часто встрачающихся бактерий вошли A. baumannii (57 культур), K. pneumoniae (49 культур) и Stenotrophomonas maltophilia (10 культур). Частота выделения карбапенемрезистентных A. baumannii и K. pneumoniae составила 91,2 и 75,5 % соответственно. Резистентность к метициллину присутствовала у 100 % золотистого стафилококка и коагулазонегативных стафилококков [16–18].
К общераспространенным причинам, способствующим присоединению инфекций, связанных с оказанием медицинской помощи (ИСМП), таким как недостаточное соблюдение принципов инфекционного контроля в отношении возбудителей ИСМП в медицинских организациях, назначение антибиотикотерапии без определения чувствительности микрофлоры к антибактериальным препаратам, необоснованное или неконтролируемое лечение (самолечение) антибиотиками на амбулаторном этапе, присоединяются специфичные для моноинфекционных госпиталей факторы, например необходимость назначения при тяжелых формах COVID-19 стероидов и ингибиторов противовоспалительных цитокинов. Актуальным является анализ особенностей циркуляции резистентных к антибактериальным химиопрепаратам штаммов возбудителей внутрибольничных инфекций как важной составляющей в обеспечении эффективного инфекционного контроля за госпитальными инфекциями, в том числе в условиях пандемического распространения новой коронавирусной инфекции.
Целью настоящей работы являлось изучение этиологической структуры внебольничных пневмоний в период эпидемического распространения COVID-19, оценка рисков возникновения пневмоний, связанных с оказанием медицинской помощи.
Материалы и методы. В период со 2 по 24 декабря 2020 года в г. Ростове-на-Дону обследовано 446 больных с внебольничной пневмонией, находившихся в стационарах или на амбулаторном лечении. Критерии включения в исследование: возраст старше 18 лет, установленный диагноз внебольничной пневмонии (J 18.9) согласно Российским национальным рекомендациям по внебольничной пневмонии (2019), информированное согласие пациента на участие в исследовании. Дополнительно для оценки динамики развития условно-патогенной бактериальной микрофлоры у пациентов, а также рисков присоединения нозокомиальной инфекции в дизайн исследования были включены группы пациентов, проходившие лечение в тех же медицинских организациях в течение не менее 6 и не более 10 дней (рис. 1). Все обследуемые пациенты были разделены на три группы.
- Группа 1 – больные с диагнозом «внебольничная пневмония» (ВП). Первичный отбор проб биологического материала (БМ) проводили в первые сутки после поступления в стационар или обращения в поликлинику (всего 303 пациента). Повторный отбор проб БМ проводили через 6–10 суток после поступления в стационар или амбулаторного лечения (всего 62 пациента).
- Группа 2 – пациенты, находящиеся на лечении не менее 6 и не более 10 суток в том же отделении, в которое госпитализированы больные из группы 1 (в случае его госпитализации). Однократный отбор проб БМ проводили при поступлении пациента из группы 1 (всего 42 пациента).
- Группа 3 – пациенты, находившиеся на лечении в той же палате, что и больные группы 1. Однократный отбор проб БМ проводили через 6–10 дней совместного пребывания в палате (всего 39 пациентов).
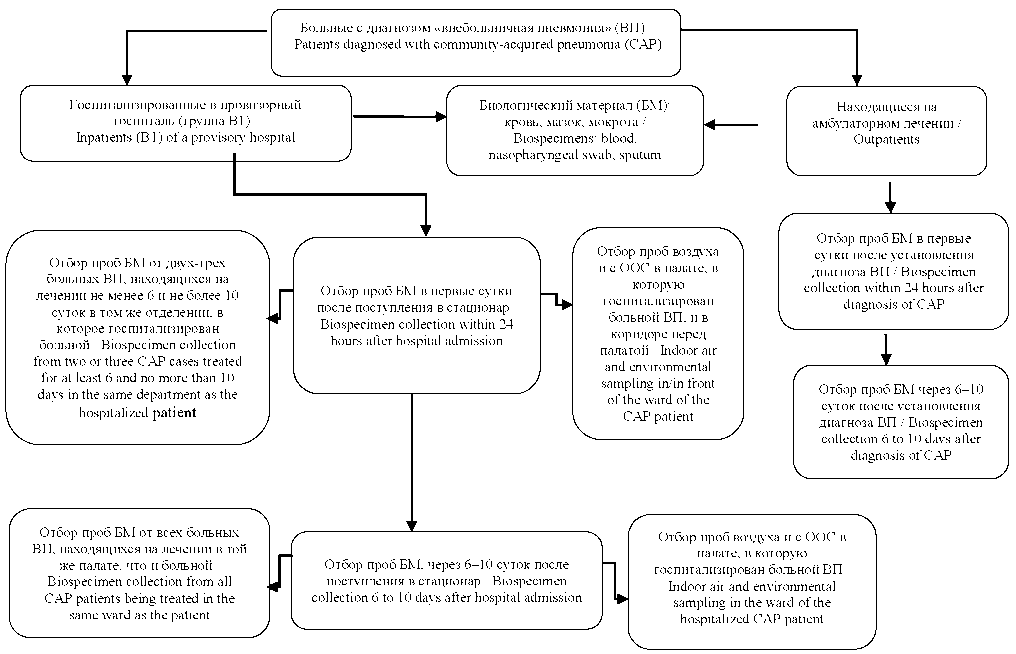
Рис. 1. Схема исследования
Fig. 1. Research process flow chart
Материал для исследования: мазки из носоглотки и мокрота, сыворотка крови. Сбор, транспортирование и исследование биоматериала соответствовали требованиям нормативно-методических документов 2 3. Всего было получено 1293 пробы пациентов, в том числе 446 мазков из носоглотки, 438 образцов мокроты, 409 образцов крови. Исследование биологического материала от пациентов проводилось на базе ФКУЗ «Ростовский-на-Дону противочумный институт» Роспотребнадзора.
Дополнительно проводили исследование проб из объектов окружающей среды (ООС): палат, смывов из аппаратов респираторной поддержки в день поступления в отделение ЛПУ пациента из группы 1 и затем через 1 неделю; исследование проводилось на базе ФБУЗ ЦГиЭ в Ростовской области.
Верификация респираторных вирусов, включая РНК SARS-CoV-2, а также M. pneumoniae, C. pneumoniae, L. pneumophila, выполнена методом ПЦР в мазках носоглотки. Сравнительный анализ результативности обнаружения РНК SARS-CoV-2 проведен путем параллельного ПЦР-исследования мазков носоглотки и мокроты, сыворотки крови. Исследование клинического материала осуществляли при помощи наборов реагентов: «РИБОпреп», «Реверта-L», «АмплиСенс ОРВИ-скрин-FL», «АмплиСенс Influenza virus A/B-FL», «АмплиСенс Mycoplasma pneumoniae / Chlamydophila pneumoniaeFL», «АмплиСенс Legionella pneumophila-FL», «Вектор-ПЦРрв-2019-nCoV-RG».
Исследование сывороток крови на наличие антител к SARS-CoV-2 проводили с использованием наборов реагентов «SARS-CoV-2-IgMИФА-БЕСТ» (АО «Вектор-Бест») и «ИФА антиSARS-CoV-2 IgG».
Проведено микроскопическое исследование мокроты, окрашенной по Граму (n = 438), посев мокроты на дифференциально-диагностические среды с определением концентрации возбудителя (n = 438). Клинически значимыми считали микроорганизмы, выделенные из мокроты в количестве ≥ 105 КОЕ/мл. Идентификацию выделенных штаммов бактерий осуществляли микробиологическими методами (окраска по Граму, морфология колоний, биохимические свойства) и с помощью времяпролетной масс-спектрометрии на приборе Autoflex (Bruker Daltonics, Германия) c программным обеспечением BioTyper 3,0. Уровень достоверности (Score) выше 2,3 свидетельствовал о точной видовой идентификации.
Резистентность к антимикробным препаратам проводили диско-диффузионным методом на среде Мюллера – Хинтона в соответствии с нормативно-методическими документами 4 5.
Анализ данных проведен с помощью пакета статистических программ Statistica, версия 10.0 (StatSoft Inc., США). Сравнение количественных показателей выполнено с применением критерия Стьюдента. Различия считались статистически значимыми при р < 0,05.
Результаты и обсуждение. На первом этапе было проведено обследование 303 пациентов с внебольничной пневмонией в первый день поступления в стационар или обращения в поликлинику. Возраст пациентов составлял от 21 года до 94 лет (медиана – 61 год). В результате исследования показано, что частота случаев ВП увеличивается пропорционально возрасту пациентов. Так, 76,7 % случаев ВП зарегистрировано у лиц старше 50 лет, при этом наибольшее (32,5 %) число заболевших отмечено среди пациентов от 60 до 69 лет. Среди обследованных 273 (90,1 %) пациента госпитализированы в медицинские организации г. Ростова-на-Дону, 30 (9,9 %) – находились на амбулаторном лечении. Наибольшее число (67,4 %) госпитализаций пациентов пришлось на 3–9-е сутки после начала заболевания независимо от выявления SARS-CoV-2.
Наличие SARS-CoV-2 лабораторно подтверждено у 108 пациентов из 303 (35,6 %). Достоверных различий в результатах исследования в зависимости от вида биологического материала не обнаружено: доля положительных мазков из носоглотки и проб мокроты составила 22,1 и 23,8 % соответственно (p > 0,05), при этом только у 31 пациента (10,2 %) РНК SARS-CoV-2 была обнаружена в обеих пробах. Корреляции между днем ПЦР-тестирования от начала появления клинических симптомов и выявлением маркеров в определенном виде биологического материала (мазке или мокроте) не обнаружено. Различия в частоте выявления РНК SARS-CoV-2 в мокроте и мазках из носоглотки были показаны нами ранее [12] и могут быть обусловлены как непродуктивным кашлем, характерным для вирусной пневмонии, так и погрешностями отбора материала, что необходимо учитывать при организации работы медицинского персонала на этом этапе. Одновременное исследование сывороток крови позволило выявить иммуноглобулины класса M у 121 пациента (39,9 %) и IgG – у 55 (18,2 %). Для зимнего периода характерен эпидемический подъем ОРВИ и гриппа среди населения. Грипп и другие острые респираторные вирусные инфекции (ОРВИ) составляют более 90 % всех инфекционных заболеваний. При массовых вспышках гриппа инфекция может охватить от 5 до 15 % населения [19][20]. В связи с этим особую актуальность представляют в период пандемии новой коронавирусной инфекции результаты исследования клинического материала на наличие вирусов гриппа, а также других возбудителей инфекций дыхательных путей вирусной природы. У 10,6 % пациентов выявлены коронавирусы типов HKU-1, OC43, HL-63 или 229Е, РС-вирусы (4,3 %), риновирусы (1,3 %) и другие возбудители респираторных заболеваний (табл. 1). Не зарегистрированы положительные результаты при исследовании на вирус гриппа типов A и B, что, вероятно, связано с соблюдением масочного режима и других противоэпидемических мероприятий. Среди пациентов с положительным результатом на SARS-CoV-2 вирусные микст-инфекции обнаружены у 28 (25,9 %) пациентов. В группе с отрицательным результатом на SARS-CoV-2 выявлено 52 пробы (26,2 %) с установленным возбудителем вирусной этиологии. Статистически достоверных различий в обнаружении респираторных микст-инфекций у пациентов SARS-CoV-2 «+» и SARS-CoV-2 «–» не выявлено (р > 0,05).
В ходе проведенного бактериологического исследования мокроты от больных у 23,7 % (72 из 303) и 37,0 % (112 из 303) пациентов с внебольничной пневмонией выявлены возбудители бактериальной и грибковой природы соответственно (табл. 2), достоверных различий коинфицирования в группах с положительным и отрицательным результатом исследования на SARS-CoV-2 нами также не выявлено (p > 0,05). В структуре изолированной микрофлоры превалировали грибы рода Candida, среди которых 72,9 % пришлось на долю C. albicans. Кроме того, были выделены клинические штаммы C. glabrata, C. dubliniensis, C. krusei, C. parakrusei, C. inconspicua, C. tropicalis. Наиболее частым этиологическим агентом ВП бактериальной природы являлись плазмокоагулирущие стафилококки (S. aureus), которые обнаружены у 30 (9,9 %) пациентов. Из условно-патогенных стрептококков только у двух пациентов с отрицательным результатом на SARS-CoV-2 был изолирован S. pneumoniae. Из представителей семейства Enterobacteriaceae наиболее часто обнаруживали E. coli и K. pneumoniae. Необходимо отметить, что достоверно чаще изолировали культуры неферментирующих грамотрицательных бактерий (НГБО) от пациентов с лабораторно подтвержденным COVID-19 (p < 0,05), преимущественно P. aeruginosa и A. baumannii.
Пациенты, проходившие лечение в стационаре, через 6–10 дней обследовались повторно (n = 62). В результате присоединение вторичной инфекции было отмечено у 51,6 % пациентов. Из них 16,1 % (10 человек) составили пациенты с лабораторно подтвержденным COVID-19, 35,5 % (22 человека) – с отрицательными результатами исследования на SARS-CoV-2. У последней группы превалировало присоединение возбудителей, относящихся к НГОБ (A. baumannii, и P. aeruginosa) и K. pneumoniae (табл. 3), в том числе характеризующихся полирезистентностью к антибактериальным препаратам.
Таблица 1. Этиологический спектр возбудителей вирусной природы
Table 1. Etiological spectrum of viral pathogens
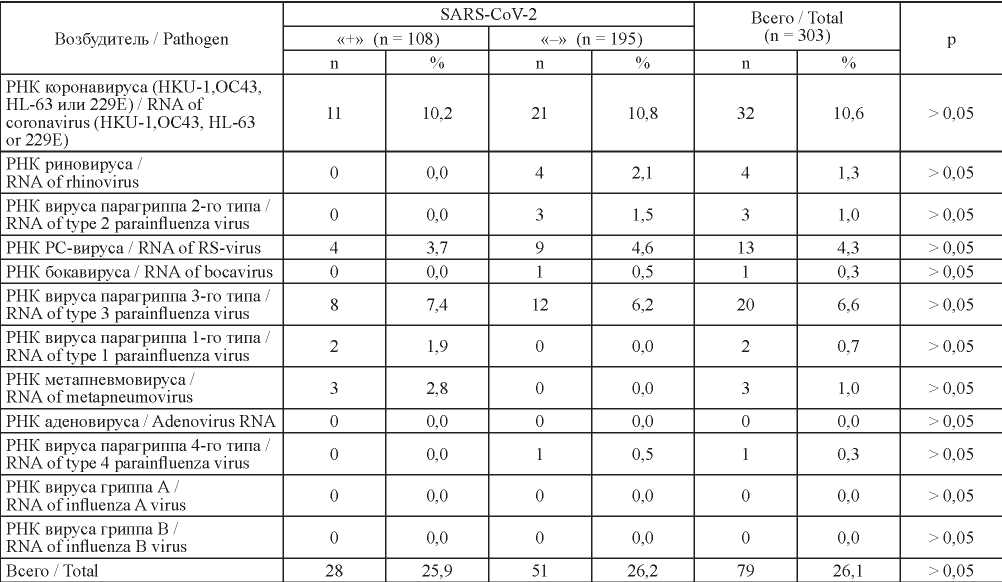
Примечание: n – количество наблюдений; р – статистическая значимость различий в группах SARS-CoV-2 «+» и SARS-CoV-2 «–».
Note: n – number of observations; p – statistical significance of differences between SARS-CoV-2 positive and negative groups.
Таблица 2. Этиологически значимые микроорганизмы, изолированные из мокроты больных внебольничными пневмониями
Table 2. Etiologically significant microorganisms isolated from sputum of patients with community-acquired pneumonia
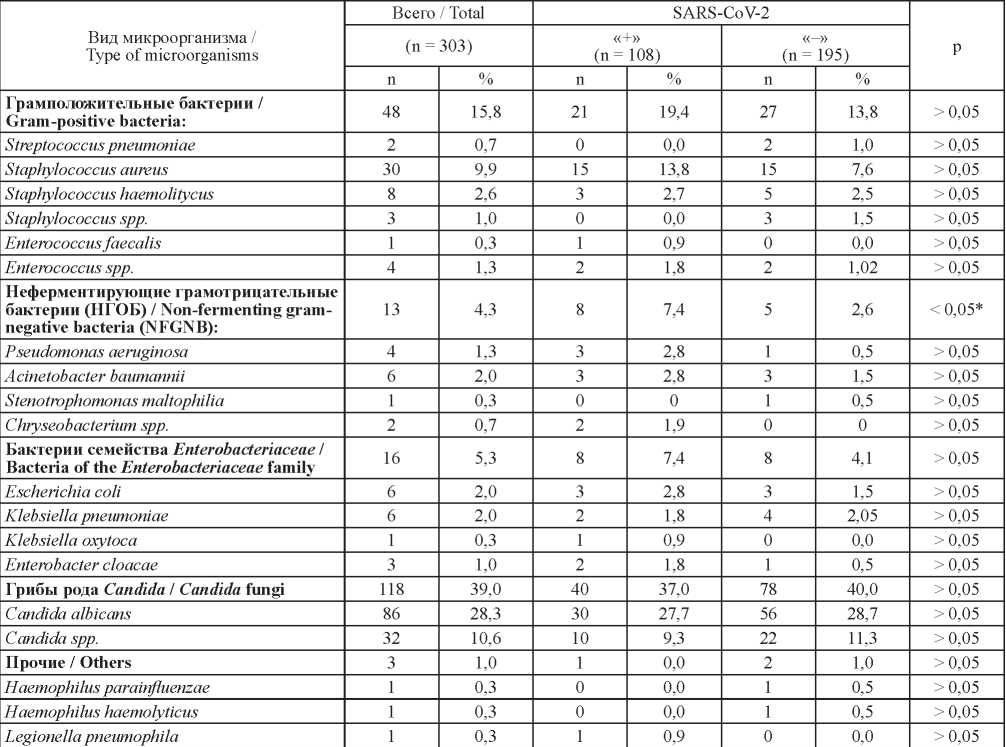
Примечание: n – количество наблюдений; р – статистическая значимость различий в группах SARS-CoV-2«+» и SARS-CoV-2«–»; * – статистически значимые различия.
Note: n – number of observations; p – statistical significance of differences between SARS-CoV-2 positive and negative groups; * – statistically significant differences.
Таблица 3. Вторичная инфекция после госпитализации
Table 3. Rates of secondary (hospital-acquired) infection
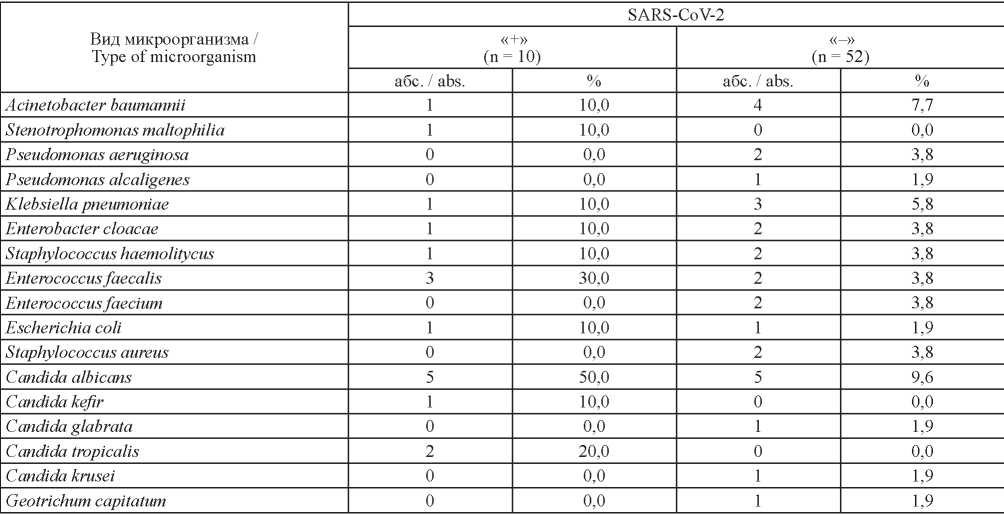
Присоединение вторичной инфекции у пациентов, находящихся на лечении, может быть обусловлено разными сценариями: это и патологическое развитие доминирующей микрофлоры слизистых верхних дыхательных путей, обеспечивающей нормобиоценоз у здоровых людей, чему способствует назначение пациентам стероидов и ингибиторов провоспалительных цитокинов, а также эмпирическое применение антибиотиков у пациентов с внебольничными пневмониями, в том числе ассоциированными с COVID-19. В то же время несоблюдение в должном объеме принципов противоэпидемического режима и инфекционной безопасности, в первую очередь гигиены рук в отношении ИСМП в ЛПУ, также может служить причиной развития внутрибольничной пневмонии у пациентов.
Для определения источника вторичного инфицирования нами были обследованы пациенты, проходившие лечение в тех же стационарах до поступления исследуемой группы или одновременно с ними, а также ООС (смывы с поверхностей и медицинского оборудования) в пяти стационарах, где проходили лечение пациенты с внебольничными пневмониями. Всего было исследовано 108 смывов с поверхностей и 28 образцов из воздуха. Из них не соответствовали требованиям нормативных документов6 5 смывов, контаминированных S. aureus и БГКП, и 2 пробы воздуха (S. aureus). В одной пробе (смыв) была обнаружена РНК вируса гриппа А(H1N1) pdm09. Все нестандартные образцы исследовались на резистентность к антимикробным препаратам. Помимо этого, на резистентность исследовались выделенные штаммы, не входящие в нормируемые показатели. В результате в медицинской организации «a» были изолированы полирезистентные штаммы S. haemolyticus и A. baumannii. В этом учреждении были зафиксированы случаи вторичного инфицирования пациентов указанными возбудителями. При исследовании биологического материала от контактных лиц (группы 2 и 3) возбудители нозокомиальных бактериальных инфекций выявлены не были, что свидетельствует об отсутствии перекрестного инфицирования пациентов (рис. 2).
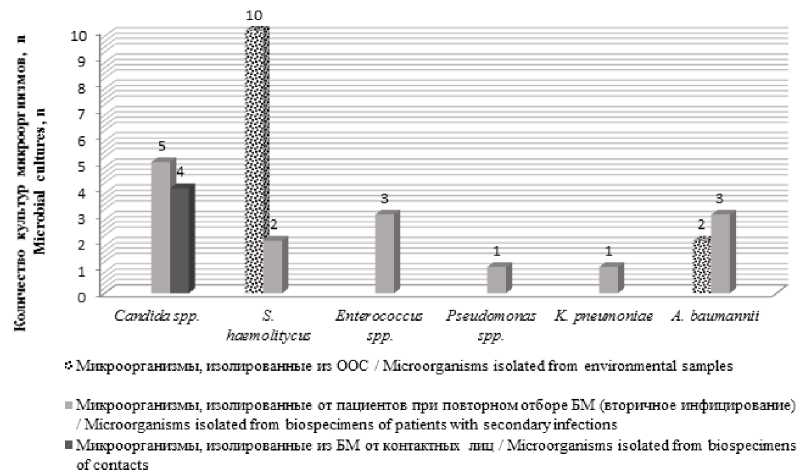
Рис. 2. Результаты микробиологического исследования БМ от пациентов и проб из ООС в стационаре МО «a»
Fig. 2. Results of microbiological testing of patients’ biospecimens and environmental samples in Hospital “а”
Заключение. Таким образом, результаты исследования свидетельствуют о том, что доля внебольничных пневмоний, ассоциированных с верифицированными случаями COVID-19, составляет 35,6 %, что ниже по сравнению с нашими предыдущими исследованиями, проведенными в августе 2020 года [12]. Если в летний период на фоне роста заболеваемости COVID-19 в Ростовской области наиболее часто этиологическим агентом ВП бактериальной природы являлись бактерии рода Streptococcus как у пациентов с ВП, ассоциированной с COVID-19, так и у пациентов с отрицательным результатом на SARS-CoV-2, то в декабре 2020 года от пациентов с новой коронавирусной инфекцией стрептококки выделены не были.
В структуре микробиоты превалируют грибы рода Candida и плазмокоагулирущие стафилококки. Достоверно чаще от пациентов с лабораторно подтвержденным COVID-19 изолировали культуры неферментирующих грамотрицательных бактерий. У 51,6 % пациентов, проходивших лечение в стационаре, отмечено вторичное коинфицирование, вероятно, связанное с объектами внешней среды или с передачей инфекции от персонала. Передача ИСМП между пациентами не установлена. В отдельных ЛПУ имеют места случаи обнаружения возбудителей ИСМП у пациентов в течение 6–10 дней пребывания в стационаре, что диктует необходимость усиления контроля над противоэпидемическим режимом в стационарах.
Дальнейшее изучение штаммов бактерий, вызвавших коинфекцию с возбудителем новой коронавирусной инфекции у пациентов, в том числе их генетическое и протеомное типирование, возможно, позволит выявить клоны, определяющие синергическое бактериально-вирусное взаимодействие при развитии внебольничной пневмонии, что, в свою очередь, позволит оценить эпидемиологические риски развития осложненных случаев COVID-19.
1. О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2019 году: Государственный доклад. М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2020. 299 с.
2. МУК 4.2.3115–13 «Лабораторная диагностика внебольничных пневмоний». М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2014. 39 с.
3. МР 4.2.0114–16 «Лабораторная диагностика внебольничной пневмонии пневмококковой этиологии». М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2017. 64 с.
4. МУК 4.2.1890–04 «Определение чувствительности микроорганизмов к антибактериальным препаратам». М.: Федеральный центр госсанэпиднадзора Минздрава России, 2004. 91 с.
5. Клинические рекомендации «Определение чувствительности микроорганизмов к антимикробным препаратам» (версия 2018-03).
6. СанПиН 2.1.3.2630–10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность». М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2010. 255 с.
Список литературы
1. Baiou A, Elbuzidi AA., Bakdach D, et al. Clinical characteristics and risk factors for the isolation of multi-drug-resistant Gram-negative bacteria from critically ill patients with COVID-19. J Hosp Infect. 2020;110:165–171. doi: 10.1016/j.jhin.2021.01.027
2. Atzrodt С, Maknojia I, McCarthy RDP, et al. A Guide to COVID-19: a global pandemic caused by the novel coronavirus SARS-CoV-2. FEBS J. 2020;287(17):3633–3650. doi: 10.1111/febs.15375
3. Wang T, Zhao M, Ye P, Wang Q, Zhao Y. Integrated bioinformatics analysis for the screening of associated pathways and therapeutic drugs in coronavirus disease 2019. Arch Med Res. 2021;52(3):304–310. doi: 10.1016/j.arcmed.2020.11.009
4. Arentz M, Yim E, Klaff L, et al. Characteristics and outcomes of 21 critically ill patients with COVID-19 in Washington State. JAMA. 2020;323(16):1612–1614. doi: 10.1001/jama.2020.4326
5. Lai CC, Wang CY, Hsueh PR. Co-infections among patients with COVID-19: The need for combination therapy with non-anti-SARS-CoV-2 agents? J Microbiol Immunol Infect. 2020; 53(4):505–512. doi: 10.1016/j.jmii.2020.05.013
6. Wu C, Chen X, Cai Y, et al. Risk factors associated with acute respiratory distress syndrome and death in patients with coronavirus disease 2019 pneumonia in Wuhan, China. JAMA Intern Med. 2020;180(7):934–943. doi: 10.1001/jamainternmed.2020.0994
7. Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020;395(10229):1054-1062. doi: 10.1016/S0140-6736(20)30566-3
8. Loosli CG, Stinson SF, Ryan DP, Hertweck MS, Hardy JD, Serebrin R. The destruction of type 2 pneumocytes by airborne influenza PR8-A virus; its effect on surfactant and lecithin content of the pneumonic lesions of mice. Chest. 1975; 67(2 Suppl):7S–14S. doi: 10.1378/chest.67.2_supplement.7s
9. Rudd JM, Ashar HK, Chow VT, Teluguakula N. Lethal synergism between influenza and Streptococcus pneumoniae. J Infect Pulm Dis. 2016;2(2):10.16966/2470–3176.114. doi: 10.16966/2470-3176.114
10. Harford CG, Leidler V, Hara M. Effect of the lesion due to influenza virus on the resistance of mice to inhaled pneumococci. J Exp Med. 1949;89(1):53–68. doi: 10.1084/jem.89.1.53
11. McCullers JA. The co-pathogenesis of influenza viruses with bacteria in the lung. Nat Rev Microbiol. 2014;12(4):252–62. doi: 10.1038/nrmicro3231
12. Попова А.Ю., Ежлова Е.Б., Демина Ю.В. и др. Особенности этиологии внебольничных пневмоний, ассоциированных с COVID-19 // Проблемы особо опасных инфекций. 2020. № 4. С. 99–105. doi: 10.21055/0370-1069-2020-4-99-105.
13. Memish ZA, Perlman S, Van Kerkhove MD, Zumla A. Middle East respiratory syndrome. Lancet. 2020;395(10229):1063–1077. doi: 10.1016/S0140-6736(19)33221-0
14. Lima WG, Brito JCM, da Cruz Nizer WS. Ventilatorassociated pneumonia (VAP) caused by carbapenem-resistant Acinetobacter baumannii in patients with COVID-19: Two problems, one solution? Med Hypotheses. 2020;144:110139. doi: 10.1016/j.mehy.2020.110139
15. Cultrera R, Barozzi A, Libanore M, et al. Co-infections in critically ill patients with or without COVID-19: A comparison of clinical microbial culture findings. Int J Environ Res Public Health. 2021;18(8):4358. doi: 10.3390/ijerph18084358
16. Li J, Wang J, Yang Y, et al. Etiology and antimicrobial resistance of secondary bacterial infections in patients hospitalized with COVID-19 in Wuhan, China: a retrospective analysis. Antimicrob Resist Infect Control. 2020;9(1):153. doi: 10.1186/s13756-020-00819-1
17. Durán-Manuel EM, Cruz-Cruz C, Ibáñez-Cervantes G, et al. Clonal dispersion of Acinetobacter baumannii in an intensive care unit designed to patients COVID-19. J Infect Dev Ctries. 2021;15(1):58–68. doi: 10.3855/jidc.13545
18. Маржохова А.Р., Плоскирева А.А., Балагова Л.Э. Клинико-лабораторная характеристика острых респираторных вирусных инфекций по данным инфекционного стационара г. Нальчика // Современные проблемы науки и образования. 2020. № 4. С. 133–133. doi 10.17513/spno.30052
19. Селькова Е.П., Гренкова Т.А., Гудова Н.В., Оганесян АС. Итоги эпидсезона 2017/18 гг. по гриппу и острой респираторной вирусной инфекции. Особенности этиотропной терапии. // РМЖ. Медицинское обозрение. 2018. Т. 2. № 11. С. 49–53.
20. Uphoff H, Cohen J-M, Fleming D, Noone A. Harmonisation of national influenza surveillance morbidity data from EISS: a simple index. Euro Surveill. 2003;8(7):156–64. doi: 10.2807/esm.08.07.00420-en
Об авторах
А. Ю. ПоповаРоссия
Попова Анна Юрьевна – д-р мед. наук, профессор, руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, главный государственный санитарный врач Российской Федерации; заведующий кафедрой организации санитарно-эпидемиологической службы ФГБОУ Российская медицинская академия непрерывного профессионального образования Минздрава России
пер. Вадковский, д. 18, г. Москва, 127994
ул. Баррикадная, д. 2/1, г. Москва, 125993
Е. Б. Ежлова
Россия
Ежлова Елена Борисовна – канд. мед. наук, заместитель руководителя
пер. Вадковский, д. 18, г. Москва, 127994
Ю. В. Демина
Россия
Демина Юлия Викторовна – д-р мед. наук, заместитель начальника управления эпидемиологического надзора Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, профессор кафедры организации санитарно-эпидемиологической службы ФГБОУ Российская медицинская академия непрерывного профессионального образования Минздрава России
пер. Вадковский, д. 18, г. Москва, 127994
ул. Баррикадная, д. 2/1, г. Москва, 125993
А. К. Носков
Россия
Носков Алексей Кимович – канд. мед. наук, директор
ул. М. Горького, д. 117/40, г. Ростов-на-Дону, 344002
Е. В. Ковалев
Россия
Ковалев Евгений Владимирович – руководитель
ул. 18-я линия, д. 17, г. Ростов-на-Дону, 344019
Г. В. Карпущенко
Россия
Карпущенко Гарри Викторович – канд. мед. наук, главный врач
ул. 7-я линия, д.67, г. Ростов-на-Дону, 344019
О. С. Чемисова
Россия
Чемисова Ольга Сергеевна – канд. биол. наук, заведующая музеем живых культур
ул. М. Горького, д. 117/40, г. Ростов-на-Дону, 344002
Н. Л. Пичурина
Россия
Пичурина Наталья Львовна – канд. мед. наук, заведующая лабораторией эпидемиологии особо опасных инфекций
ул. М. Горького, д. 117/40, г. Ростов-на-Дону, 344002
Н. В. Павлович
Россия
Павлович Наталья Владимировна – д-р мед. наук, заведующая лабораторией
ул. М. Горького, д. 117/40, г. Ростов-на-Дону, 344002
С. О. Водопьянов
Россия
Водопьянов Сергей Олегович – д-р мед. наук, заведующий лабораторией биохимии микробов
ул. М. Горького, д. 117/40, г. Ростов-на-Дону, 344002
Е. Н. Гудуева
Россия
Гудуева Елена Николаевна – мл. науч. сотр. музея живых культур
ул. М. Горького, д. 117/40, г. Ростов-на-Дону, 344002
С. С. Слись
Россия
Слись Сергей Сергеевич – главный специалист-эксперт отдела эпидемиологического надзора
ул. 18-я линия, д. 17, г. Ростов-на-Дону, 344019
Н. Ю. Пшеничная
Россия
Пшеничная Наталья Юрьевна – д-р мед. наук, профессор, заместитель директора по клинико-аналитической работе
ул. Новогиреевская, д. 3а, г. Москва, 111123
А. Р. Литовко
Россия
Литовко Анна Радиковна – заведующая вирусологической лабораторией
ул. 7-я линия, д.67, г. Ростов-на-Дону, 344019
Н. Ю. Асмолова
Россия
Асмолова Наталья Юрьевна – врач-вирусолог вирусологической лаборатории
ул. 7-я линия, д.67, г. Ростов-на-Дону, 344019
Рецензия
Для цитирования:
Попова А.Ю., Ежлова Е.Б., Демина Ю.В., Носков А.К., Ковалев Е.В., Карпущенко Г.В., Чемисова О.С., Пичурина Н.Л., Павлович Н.В., Водопьянов С.О., Гудуева Е.Н., Слись С.С., Пшеничная Н.Ю., Литовко А.Р., Асмолова Н.Ю. Этиология внебольничных пневмоний в период эпидемического распространения Covid-19 и оценка риска возникновения пневмоний, связанных с оказанием медицинской помощи. Здоровье населения и среда обитания – ЗНиСО. 2021;(7):67-75. https://doi.org/10.35627/2219-5238/2021-29-7-67-75
For citation:
Popova A.Yu., Ezhlova E.B., Demina Yu.V., Noskov A.K., Kovalev E.V., Karpushchenko G.V., Chemisova O.S., Pichurina N.L., Pavlovich N.V., Vodopyanov S.O., Gudueva E.N., Slis S.S., Pshenichnaya N.Yu., Litovko A.R., Asmolova N.Yu. Etiology of Community-Acquired Pneumonia during the Epidemic Spread of COVID-19 and Healthcare-Associated Pneumonia Risk Assessment. Public Health and Life Environment – PH&LE. 2021;(7):67-75. (In Russ.) https://doi.org/10.35627/2219-5238/2021-29-7-67-75









.png)



























